HARTFORD.- El Fiscal General William Tong se unió esta semana a una demanda federal multiestatal contra la U.S. Food & Drug Administration (FDA), acusándola de seleccionar uno de los dos fármacos utilizados para los abortos farmacológicos para una regulación excesivamente onerosa, a pesar de la amplia evidencia de que el fármaco es más seguro que el Tylenol.
Los fiscales generales también han presentado un requerimiento judicial preliminar en el que solicitan al tribunal que detenga la aplicación de las restricciones de la FDA sobre la mifepristona mientras dure el caso.
“La mifepristona es más segura que el Tylenol. A pesar de ello, la FDA impone restricciones innecesarias reservadas a algunos de los medicamentos de mayor riesgo, incluido el fentanilo. Algunas de estas restricciones implican la recopilación innecesaria de datos y certificaciones que pueden asustar a las pacientes y prescriptores preocupados por la privacidad y la seguridad. Nuestra demanda pretende bloquear estas restricciones innecesarias e ilegales y garantizar que la regulación del aborto farmacológico se base estrictamente en la ciencia y la seguridad”, declaró Tong.
De los más de 20 mil fármacos aprobados por la FDA, sólo 60 incluida la mifepristona, están sujetos a un conjunto único de restricciones conocidas como las Risk Evaluation & Mitigation Strategies (REMS).
Se supone que las restricciones REMS se aplican a los fármacos intrínsecamente peligrosos, como los opioides, como el fentanilo, y los sedantes en dosis altas utilizados por pacientes psiquiátricos, entre otros.
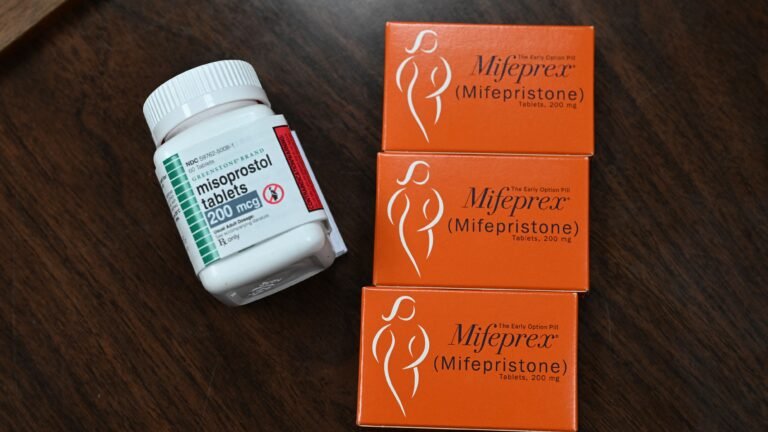
El régimen aprobado por la FDA para el aborto con medicamentos incluye una dosis de mifepristona, seguida de un segundo fármaco, el misoprostol.
Para recetar mifepristona, los profesionales sanitarios deben recibir previamente una certificación especial del distribuidor del fármaco.
Para recibir la receta, pacientes y proveedores deben firmar un acuerdo que certifique que la paciente ha decidido tomar los fármacos para interrumpir su embarazo, independientemente de si desea abortar o está recibiendo tratamiento por un aborto espontáneo, que es otro uso habitual de la mifepristona. Debe incluirse una copia de este acuerdo en la historia clínica de la paciente.
Para dispensar mifepristona, las farmacias también deben estar especialmente certificadas antes de poder dispensar una receta.
La demanda afirma que las restricciones a la prescripción y dispensación de mifepristona son indebidamente gravosas, perjudiciales e innecesarias, y exponen a proveedores y pacientes a riesgos innecesarios para su privacidad y seguridad. Los riesgos se ven exacerbados por la creciente criminalización y penalización del aborto en todo el país a raíz de la decisión del Tribunal Supremo de los Estados Unidos en el caso Dobbs contra Jackson Women’s Health.
El caso Dobbs revocó casi medio siglo de precedentes, eliminando el derecho constitucional al aborto reconocido por la decisión del tribunal en el caso Roe contra Wade.
La divulgación de la certificación de un proveedor o una farmacia para recetar mifepristona, o el acuerdo de una paciente para recibirla, todo ello exigido por la FDA, podría exponerles a la violencia, acoso o abusos.
Esta documentación también puede utilizarse para amenazar a proveedores o pacientes con responsabilidades legales en estados con leyes antiabortistas extremas, indicó Tong.
La FDA aprobó el uso de mifepristona en los Estados Unidos en combinación con misoprostol para abortos farmacológicos en 2000.
Antes de su aprobación en los Estados Unidos, la mifepristona se utilizaba ampliamente en Europa, empezando en Francia a finales de la década de 1980. Desde su aprobación por la FDA, la mifepristona se ha utilizado de forma segura más de 5 millones de veces en los Estados Unidos.
La propia FDA reconoció que “las complicaciones graves han demostrado ser extremadamente raras” con la mifepristona.
En la demanda, los fiscales generales señalaron que la mifepristona se asocia a menos efectos secundarios graves y muertes que medicamentos comunes como el Tylenol o la Viagra, ninguno de los cuales está regulado por las restricciones REMS.
Según la FDA, ni una sola muerte puede atribuirse a la mifepristona durante toda su historia de uso en Estados Unidos.
A pesar del historial de seguridad extremadamente sólido de la mifepristona, la FDA se ha negado repetidamente a eliminar las restricciones REMS sobre el medicamento, finalizó Tong.